[研究成果] 秋山班の研究がSTEM CELLS Translational Medicine誌に掲載されました!
2020.12.21
Akiyama T*, Sato S, Ko SBH, Sano O, Sato S, Saito M, Nagai H, Ko MSH, Iwata H* (*corresponding author), Synthetic mRNA‐based differentiation method enables early detection of Parkinson’s phenotypes in neurons derived from Gaucher disease‐induced pluripotent stem cells. STEM CELLS Translational Medicine. 2020 Dec 20. in press.
プレスリリースはこちらから。
合成mRNA分化誘導法でパーキンソン病の誘因物質を早期に検出
1.研究の背景と概要
神経変性疾患であるパーキンソン病は、加齢とともに罹患率・有病率が増加し、65歳以上の100人に1人がかかる病気です。急速に高齢化が進む日本では、パーキンソン病患者の数が増え続けることが予想されており、その病態解明と治療法の開発が急務となっています。パーキンソン病の発症には、中脳にある黒質神経細胞(ドーパミン神経)におけるαシヌクレインの凝集化が深く関与しますが、その原因については未だ不明な点が多く残されています。今回の研究では、パーキンソン病を併発しやすい先天性代謝異常疾患ゴーシェ病に着目しました。ゴーシェ病は、糖脂質グリコシルセラミドの分解酵素であるGBA遺伝子の変異によって起こります。糖脂質の分解ができず、肝臓、脾臓の肥大や、貧血、血小板減少といった症状を主に呈しますが、神経症状が現れる場合もあり、その有無と重症度によって3つのタイプに分類されます(I~III型)。そのうち比較的軽度なI型ゴーシェ病は神経症状を伴わないものの、高齢になるとパーキンソン病の発症リスクが9%~12%と非常に高くなることが知られています。脳内における糖脂質の過度な蓄積がパーキンソン病の発症に影響することが示唆されますが、その機序についてはよくわかっていません。
今回の研究では、武田薬品工業との共同で、I型ゴーシェ病患者由来のiPS細胞から作製した神経細胞を用いて糖脂質の蓄積とαシヌクレインの関連性について調べました。
2.研究の成果と意義
当研究室では、以前、iPS細胞から神経細胞を効率よく作製する分化誘導技術を開発しました。この技術の特徴は、合成mRNAを導入することにより細胞内の遺伝子発現を簡便に操作できる点です。合成mRNAには転写因子がコードされており、神経分化を促進させる働きがあります。iPS細胞へ導入されたmRNAは数時間でタンパク質に翻訳されます。通常1カ月以上かかる従来の分化誘導法に比べて、合成mRNA法では1週間で神経細胞を作ることができるメリットがあります。今回の研究では、この技術を応用させ、ゴーシェ病患者由来のiPS細胞からドーパミン神経への分化誘導を行いました。また従来法でも分化誘導を行い、病態に関わる表現型が現れる時期を比較しました。
まず従来の方法で作製した神経細胞では、分化開始後60日以降に糖脂質の蓄積が起こることが質量分析法により明らかになりました。この手法では神経細胞ができるまでに1か月程度かかるため、表現型の検出にはさらに時間を要することが分かりました。これに対し、合成mRNAを使った分化誘導法では、分化開始後わずか10日の時点で糖脂質の蓄積を確認することができました。さらに、この時点では、αシヌクレインの凝集は未検出でしたが、それに関わるαシヌクレインのリン酸化修飾が亢進されており、神経変性を起こしやすい状態にあることが分かりました。また、正常なGBA遺伝子を強制発現させ糖脂質の分解を促すとαシヌクレインのリン酸化を抑制できたことから、糖脂質の蓄積がパーキンソン病の発症に直接関与することが示唆されました。
以上の結果により、合成mRNA分化法は短期間の分化を可能とするだけでなく、疾患に関わる表現型の迅速な再現にも有効であることが示されました(図1)。本研究成果はスピードの向上が求められる創薬開発への応用が期待されます。
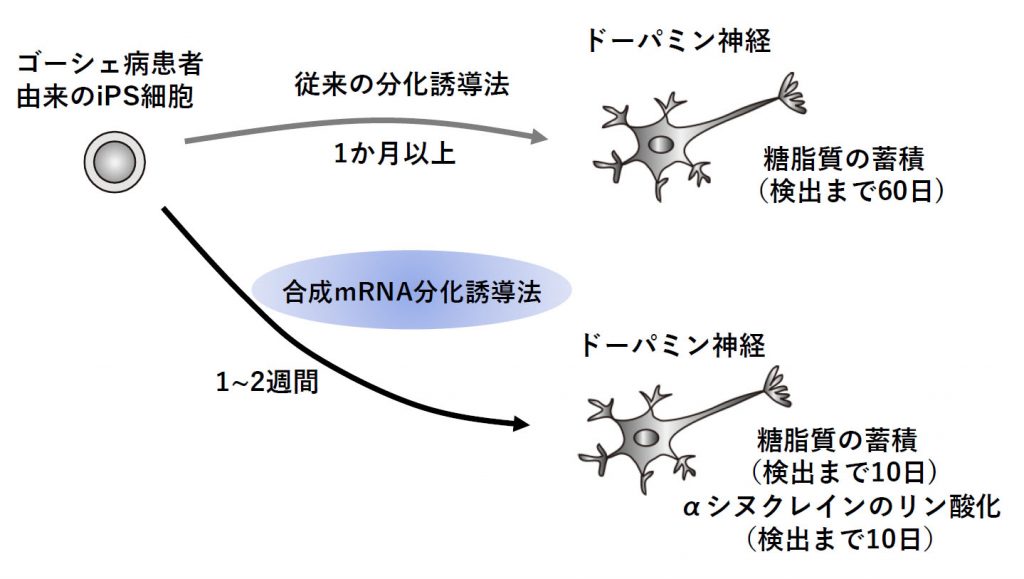
図1 本研究の概要
本研究は、「武田薬品工業オープンイノベーションプログラムCOCKPI-T」、「坂口光洋記念慶應義塾医学振興基金」、科学研究費補助金(JP19K06492, JP20H05395, JP20H04929)の支援によって行われました。