[研究成果] 班友になられた仙石班の研究がNat Commun誌に掲載されました!
2021.11.17
Sato K, Kumar A, Hamada K, Okada C, Oguni A, Machiyama A, Sakuraba S, Nishizawa T, Nureki O, Kono H, Ogata K, Sengoku T. Structural basis of the regulation of the normal and oncogenic methylation of nucleosomal histone H3 Lys36 by NSD2. Nat Commun. 12(1):6605 (2021)
ヒストンメチル化酵素NSD2は発がん性変異により安全装置が外れ、制御不能になる
横浜市立大学大学院医学研究科 生化学 仙石 徹 講師、佐藤 光 助教、緒方 一博 教授、同大学大学院生命医科学研究科 西澤 知宏 教授、量子科学技術研究開発機構 量子生命・医学部門量子生命科学研究所生体分子シミュレーショングループ Amarjeet Kumar 博士研究員、河野 秀俊 グループリーダー、東京大学理学系研究科 生物科学専攻 濡木 理 教授らの研究グループは、血液がん発症に関わるヒストンメチル化酵素NSD2の発がん性変異体の活性亢進メカニズムを明らかにしました。この発見はNSD2の変異が関係する血液がんの治療薬開発につながるものと期待されます。
研究成果のポイント
- 血液がん発症に関わるヒストンメチル化酵素NSD2と基質ヌクレオソームとの複合体の立体構造をクライオ電子顕微鏡を用いて解明
- NSD2の発がん性変異による活性亢進メカニズムを解明
- NSD2変異が関係する血液がんの治療薬開発への貢献が期待される
研究背景
近年、一部の血液がんの発症には、ヌクレオソーム中のヒストンH3をメチル化する酵素NSD2の異常な活性亢進が関わっていることがわかってきました。例えば、リンパ性白血病の一部ではNSD2にメチル化活性を亢進させるアミノ酸変異(E1099K)が見つかっています。一方、多発性骨髄腫の20%では染色体転座t(4;14)によりNSD2タンパク質の量が異常に増加しています。
これらの症例では、NSD2の基質であるヒストンH3の36番目のリジン残基(H3K36)が異常に高いレベルでメチル化を受けています。このH3K36のメチル化は遺伝子発現の調節にかかわることが知られており、H3K36メチル化の異常は遺伝子発現パターンを変化させることで造血細胞のがん化につながると考えられています。
そこで、本研究ではこのNSD2の発がん性変異E1099Kがどのようにヒストンメチル化活性を異常亢進させるかを調べました。
研究内容
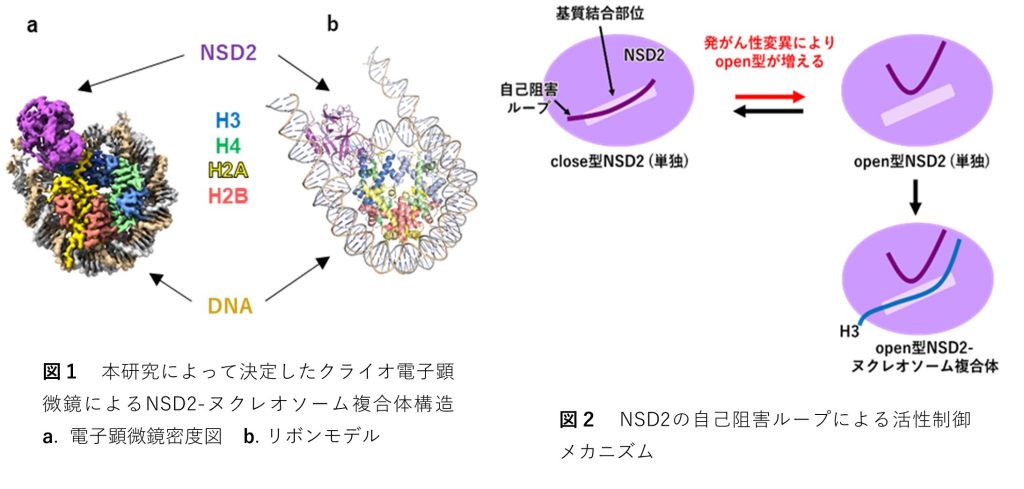
本研究ではクライオ電子顕微鏡を用いた単粒子解析法を用い、NSD2とヌクレオソームとの複合体の立体構造を決定しました(図1)。既に解かれていたNSD2の単独構造(図2左上)では、自己阻害ループと呼ばれるNSD2の一部の領域が基質結合部位を覆っており(close型)、H3の結合を妨げていました。一方、ヌクレオソームとの複合体(図2右下)では、基質結合部位は自己阻害ループに覆われておらず(open型)、H3が基質結合部位に結合していることが明らかとなりました。
さらに分子動力学シミュレーションを用いて解析したところ、発がん性変異を持たないNSD2では自己阻害ループが基質結合部位に常に留まっていました。これらの解析から、自己阻害ループがいわば安全装置として働き、NSD2による異常なメチル化を防いでいることがわかりました。
一方、発がん性変異E1099Kを有するNSD2についても分子動力学シミュレーションを用いて解析したところ、発がん性変異E1099Kが存在すると自己阻害ループが外れてopen型の構造をとりやすくなっていることがわかりました。すなわち、発がん性変異によりNSD2の安全装置が外れ、NSD2の活性が制御不能になることで、H3K36のメチル化レベルが異常に上昇し、ひいては細胞のがん化につながる変化を引き起こすことが考えられます。
今後の展開
本研究で解明した立体構造に基づき、NSD2のヒストンメチル化活性を抑える薬剤を設計することで、NSD2の活性亢進あるいは発現亢進による血液がんに対する治療法の進展が期待されます。